Využití kmenových buněk v léčbě poranění rohovky

Poranění hlubokých struktur oka koně je noční můrou chovatelů, protože se obvykle jedná o zranění, která zrak koně v různém rozsahu nenávratně poškodí. Jistou naději přináší mezenchymální kmenové buňky. Ty totiž představují zajímavou možnost terapie mnoha patologických procesů postihujících rohovku.
Rohovka je průhledná hmota chránící povrch oka a je složkou jeho světlolomného systému. Skládá se z epitelu, stromatu, Descemetovy membrány a endotelu. Epitel tvoří 7–15 vrstev buněk, jež se obnovují co 7–10 dní. Mezi bazální vrstvou epitelu a bělimou se nachází vrstva tzv. limbálních epiteliálních kmenových buněk, jež se uplatňuje v obnově epitelu. Stroma tvoří pravidelně uspořádaná kolagenní vlákna, extracelulární matrix (ECM; amorfní hmota tvořená látkami, jako jsou proteoglykany, glykosaminoglykany, kyselina hyaluronová) a buňky, tzv. keratocyty. Keratocyty jsou specializované fibroblasty vyskytující se ve stromatu rohovky, jež se účastní hojení, tvorby komponent rohovky a udržují její transparenci. Z klidového stavu jsou aktivovány zánětem nebo zraněním, čímž vzniká jejich myofibroblastický fenotyp. Endotel je tvořen jedinou vrstvou buněk, jež mají malou až nulovou regenerační kapacitu. Rohovka nemá cévní zásobení a lymfatickou drenáž, což způsobuje její pomalejší hojení.
![]()
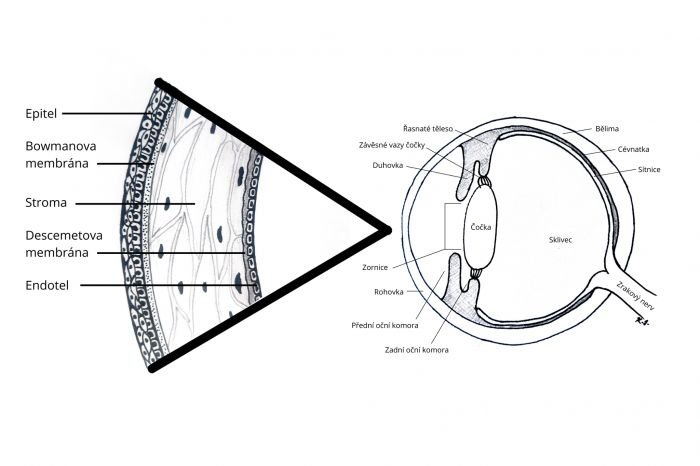
Poškození epitelu aktivuje mechanismy, jež vedou k migraci, proliferaci a adherenci nepoškozených epiteliálních buněk. Poškozením hlubších vrstev dochází k aktivaci dalších hojících mechanismů v epiteliální a stromální vrstvě včetně aktivace stromálních keratocytů produkujících ECM. Po poranění epitelu rohovky dojde k uvolnění prozánětlivých faktorů a prozánětlivý stav, pokud je nekontrolován, vede k inhibici reepitelizace, zvýšené vaskularizaci a nekontrolované aktivaci stromálních fibroblastů na myofibroblasty produkující neorganizovanou ECM. Správně probíhající hojení vede k uzavření epiteliálního defektu a redukci myofibroblastů. Bohužel nadměrná aktivace myofibroblastů může následně vést ke vzniku jizvy nebo syntéze excesivní a nevhodné ECM, což vede ke ztrátě transparence rohovky až oslepnutí.
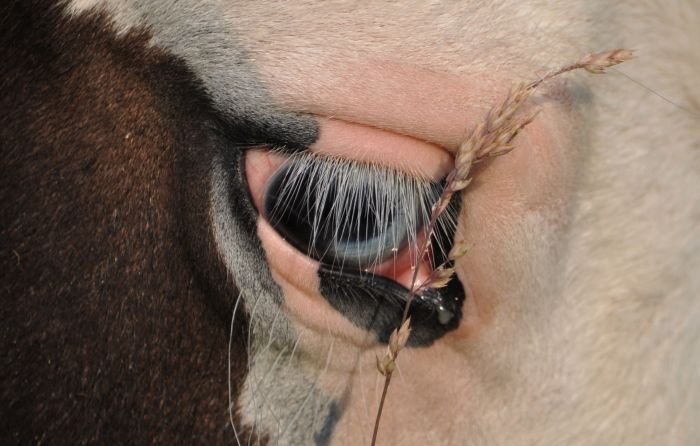
Rohovka je přímo vystavena vnějšímu prostředí a chrání oko před vniknutím cizího materiálu, nečistot, bakterií, virů atd. Přímé vystavení okolnímu prostředí vede k poměrně častým zraněním této tkáně. Kůň se řadí mezi suchozemské savce s největšíma očima umístěnýma laterálně. Jejich rohovka se hojí pomaleji než u jiných zvířat, což vede k častějšímu výskytu dalších komplikací a infekcí. Nevýhodou je i to, že oční problém u koně je jeho majitelem zaznamenán často později než u malých zvířat, která jsou s majiteli v těsnějším kontaktu. Koně mají také tendenci se plašit a jsou chováni v prostředí, ve kterém ke zranění může častěji dojít. Oko se může poranit např. o stájová vrata, sloupy, ohrady, větve stromů, kopyta jiných koní apod.
Častější jsou tupá poranění než ostrá, poměrně častým problém jsou i lacerace (natržení) víček. Léze rohovky bývají většinou superficiální (povrchové), někdy jsou ale asociovány s nitroočním poškozením, jako je uveitida, krvácení do sklivce a odchlípení retiny. Trauma bez ohledu na příčinu vede k edému rohovky, který se projeví jejím zamlžením (zvýšenou opacitou) a namodralým zbarvením.
Zánět rohovky (keratitida) tvoří u koní 35 % oftalmologických problémů a vzhledem k pomalému hojení je pro ně velmi frustrující. Průběh je většinou akutní, velmi bolestivý a projevuje se slzením, blefarospazmem, citlivostí na světlo, překrvením spojivky a zmiňovaným zamlžením rohovky. Klasická léčba se skládá z kontroly bolesti, zánětu a prevence sekundárních infekcí.
Povrchové poranění rohovky se většinou vyřeší během několika dní bez dlouhodobých následků a bez narušení vidění. V případě chronicity procesu dochází často k dalším infekcím a komplikacím vedoucím až k perforaci rohovky nebo slepotě.
Onemocnění rohovky často vedou až k nutnosti její transplantace, bohužel dárců není dostatek, a proto se hledají alternativní přístupy, jež by mohly pomoci tento problém vyřešit. Výhodou rohovky je, že je imunologicky privilegovaným orgánem.
![]()
![]() Kmenové buňky jsou buňky s časově neomezenou schopností sebeobnovy, kdy při jejich dělení vzniká buňka podobná mateřské (udržuje pool kmenových buněk) a buňka schopná diferenciace do specializovanějšího buněčného typu. Dle původu můžeme buňky dělit na embryonální a kmenové buňky vyskytující se v dospělém organismu (adultní), jež slouží k obnově orgánů a tkání. Jedním z typů adultních kmenových buněk jsou mesenchymální kmenové buňky (MSC). MSC jsou multipotentní buňky schopné diferenciace do specializovanějších buněk mezodermální linie, za určitých podmínek byla prokázána diferenciace do buněk neuroektodermální a endodermální linie, jako jsou neurony, endoteliální buňky a hepatocyty. Dle International Society of Cellular Therapy jsou definovány schopností adherence k plastům, expresí určitých povrchových markerů a schopností diferenciace do tří hlavních linií (osteoblasty, chondrocyty, adipocyty) in vitro.
Kmenové buňky jsou buňky s časově neomezenou schopností sebeobnovy, kdy při jejich dělení vzniká buňka podobná mateřské (udržuje pool kmenových buněk) a buňka schopná diferenciace do specializovanějšího buněčného typu. Dle původu můžeme buňky dělit na embryonální a kmenové buňky vyskytující se v dospělém organismu (adultní), jež slouží k obnově orgánů a tkání. Jedním z typů adultních kmenových buněk jsou mesenchymální kmenové buňky (MSC). MSC jsou multipotentní buňky schopné diferenciace do specializovanějších buněk mezodermální linie, za určitých podmínek byla prokázána diferenciace do buněk neuroektodermální a endodermální linie, jako jsou neurony, endoteliální buňky a hepatocyty. Dle International Society of Cellular Therapy jsou definovány schopností adherence k plastům, expresí určitých povrchových markerů a schopností diferenciace do tří hlavních linií (osteoblasty, chondrocyty, adipocyty) in vitro.
Kromě schopnosti diferenciace je zajímavou vlastností MSC účinek imunomodulační, protizánětlivý, regenerativní a trofický, který je zprostředkován převážně sekrecí různých látek, vylučováním exosomů nebo přímým buněčným kontaktem. Dále je důležité, že jsou schopny reagovat na různé látky a molekuly uvolňované z poškozené tkáně a v odpovědi na ně tvořit různé působky potřebné k normálnímu hojení a mohou migrovat i do místa poškození. Jsou považovány za buňky s imunologickým privilegiem.
Terapeuticky jsou MSC využívány především u nemocí muskuloskeletálního systému (např. ruptury šlach, osteoartrózy, traumata páteřní míchy), zkoumáno je i využití u nemocí s imunitním podkladem, ale také například v oftalmologii. U lidí se zmiňuje možnost terapeutické aplikace MSC v souvislosti se zraněními rohovky, poleptáním, syndromem suchého oka, insuficiencí limbálních kmenových buněk a s transplantací rohovky (jsou schopny zmírňovat reakci na transplantát).

Ve veterinární medicíně je použití MSC popsáno u léčby syndromu suchého oka a traumat rohovky psů. U koní bylo použití MSC zkoumáno v rámci equinní rekurentní uveitidy (ERU, měsíční slepota) nebo ulcerativní keratitidy. V případě ERU byla in vitro prokázána schopnost suprese určitého fenotypu T buněk uplatňujícího se v patogenezi ERU. Ve studii zaměřující se na imunitně zprostředkovanou keratitidu koní byla u 3 ze 4 zvířat pozorována redukce opacity rohovky, neovaskularizace a úprava povrchových nepravidelností rohovky po subkonjuktivální aplikaci autologních MSC z kostní dřeně. Podobného výsledku bylo dosaženo i ve studii zaměřené obecněji na ulcerativní keratitidu z různých příčin po lokální nebo intravenózní aplikaci MSC izolovaných z periferní krve. Studie zkoumající účinek MSC u traumat rohovky psů s následnými ulceracemi přinesla povzbudivé výsledky, kdy u 22 z 26 psů došlo k úplnému vyléčení ulcerací nereagujících na klasickou terapii.
Ačkoliv klinické studie zaměřující se na využití MSC u traumatických keratitid koní neexistují, je tato možnost terapie do budoucnosti zajímavá, jelikož poranění rohovky a očí postihuje i koně a je pro ně velmi frustrující – hojení je u nich pomalejší než u jiných zvířat a častěji se vyskytují sekundární infekce.
Existuje studie in vitro zkoumající vliv MSC izolovaných z kostní dřeně koní nebo supernatantu získaného během kultivace těchto buněk na hojení ran při tzv. „testu škrábanců“ (seškrábne se buněčný monolayer a pravidelně se pak posuzuje migrace buněk do defektu), v tomto případě v přítomnosti MSC nebo supernatantu. Bylo pozorováno signifikantní zlepšení hojení v přítomnosti MSC nebo supernatantu oproti kontrole (lepších výsledků bylo dosaženo při použití MSC). Výhodou supernatantu oproti MSC je jeho neimunogenita díky nepřítomnosti buněk, rychlejší dostupnost, snadnější skladování a nižší finanční náročnost.
Ve studiích na téma efektu aplikace MSC při patologických procesech na rohovce je u laboratorních zvířat popisováno snížení opacity rohovky, redukce vaskularizace, zlepšení reepitelizace. Reepitelizace je důležitá také proto, aby nedošlo k dalšímu poškozování stromatu a aktivaci myofibroblastů. Díky uvolnění imunomodulačních působků jsou MSC schopny kontrolovat a podporovat správně probíhající hojení. Jako nejvýznamnější protizánětlivé proteiny se uplatňují TSG6 (TNFα-stimulated gene-6; moduluje aktivitu neutrofilů), HGF (hepatocytegrowthfactor; protizánětlivý účinek) a antiangiogenní cytokiny bránící vaskularizaci rohovky. Zajímavé je, že ačkoliv obecně v jiných tkáních MSC podporují novotvorbu cév, tak v rohovce ji naopak inhibují. Dále na animálních modelech byla prokázána i integrace MSC do korneálního stromatu, produkce nové organizované ECM a hojení probíhalo s minimem jizev. Za určitých podmínek byla pozorována i transdiferenciace MSC do korneálních epiteliálních nebo endoteliálních buněk. Po aplikaci tyto buňky byly schopny tvořit normální ECM, jež neovlivňovala transparenci rohovky a schopnost vidění. Většina studií se ale shoduje, že samotné MSC dlouhodobě v tkáni neperzistují a jako primární mechanismus účinku MSC nejen v terapii nemocí rohovky se považuje tvorba imunomodulačních a trofických faktorů.
![]()
Aplikace MSC je považována za bezpečnou, s nízkým rizikem nežádoucích účinků. Ve studiích byly zkoušeny různé cesty aplikace (přímo do defektu, subkonjuktivální, intravenózní, na nosiči), které byly většinou všechny shledány efektivní. Výrazný rozdíl nebyl zatím nalezen ani mezi různými zdroji MSC. Jedna studie zmiňuje stejnou účinnost MSC izolovaných z kostní dřeně jako samotných limbálních epiteliálních kmenových buněk, výhodou je i jejich snadnější kultivace a větší výtěžnost. Efekt byl prokázán dokonce při použití média, ve kterém byly MSC kultivovány.
Závěrem lze říct, že použití MSC je bezpečné a pro své vlastnosti MSC představují zajímavou možnost terapie mnoha patologických procesů postihujících rohovku.
Zdroje:
- Al-Jaibaji O, Swioklo S, Connon CJ (2019): Mesenchymalstromalcellsforocularsurfacerepair. Expert OpinBiolTher., 19, 643-653. doi: 10.1080/14712598.2019.1607836.
- Davis AB, Schnabel LV, Gilger BC (2019): Subconjunctival bone marrow-derivedmesenchymal stem cell therapy as a novel treatmentalternativeforequineimmune-mediated keratitis: A case series. Vet Ophthalmol., 22, 674-682. doi: 10.1111/vop.12641.
- Falcão MSA, Brunel HDSS, Peixer MAS, Dallago BSL, Costa FF, Queiroz LM, Campbell P, Malard PF (2019): Effectofallogeneicmesenchymal stem cells (MSCs) on cornealwoundhealing in dogs. J TraditComplement Med., 10, 440-445. doi: 10.1016/j.jtcme.2019.04.006.
- Ghiasi M, Jadidi K, Hashemi M, Zare H, Salimi A, Aghamollaei H (2021): Applicationofmesenchymal stem cells in cornealregeneration. Tissue Cell., 73. doi: 10.1016/j.tice.2021.101600.
- Marfe G, Massaro-Giordano M, Ranalli M, Cozzoli E, Di Stefano C, Malafoglia V, Polettini M, Gambacurta A (2012): Bloodderived stem cells: anameliorativetherapy in veterinaryophthalmology. J Cell Physiol., 227, 1250-1256. doi: 10.1002/jcp.22953.
- Sahu A, Foulsham W, Amouzegar A, Mittal SK, Chauhan SK (2019): Thetherapeuticapplicationofmesenchymal stem cellsattheocularsurface. Ocul Surf., 17, 198-207. doi: 10.1016/j.jtos.2019.01.006.
- Saldinger LK, Nelson SG, Bellone RR, Lassaline M, Mack M, Walker NJ, Borjesson DL (2020): Horseswithequinerecurrentuveitishaveanactivated CD4+ T-cell phenotypethatcanbemodulated by mesenchymal stem cells in vitro. Vet Ophthalmol., 23, 160-170. doi: 10.1111/vop.12704.
- Sherman AB, Gilger BC, Berglund AK, Schnabel LV (2017): Effectofbonemarrow-derivedmesenchymal stem cells and stem cell supernatant on equinecornealwoundhealing in vitro. Stem Cell Res Ther., 8, 120. doi: 10.1186/s13287-017-0577-3.
MVDr. Markéta Slaná je členkou týmu projektu Avecell. AVECELL® je veterinární projekt Medicínského centra Praha, v němž se tým odborníků zaměřuje na výzkum a využití nových metod léčby pomocí aplikace kmenových buněk ve veterinární medicíně.
 Medicínské centrum Praha získalo povolení pro výrobu veterinárního léčivého přípravku (autologní mezenchymální kmenové buňky) od Ústavu pro státní kontrolu veterinárních biopreparátů a léčiv (ÚSKVBL) v květnu 2015.
Medicínské centrum Praha získalo povolení pro výrobu veterinárního léčivého přípravku (autologní mezenchymální kmenové buňky) od Ústavu pro státní kontrolu veterinárních biopreparátů a léčiv (ÚSKVBL) v květnu 2015.
Galerie






V minulém článku jste se dozvěděli něco o anatomii koňského oka a o tom, jak koně vidí. Dnes se v tomto seriálu o traumatech očí u koní zaměříme na…
Kmenové buňky a neurodegenerativní choroby – pomohou pro zlepšení paměti?
V posledních letech obrovsky vzrůstá zájem o možnost léčby některých závažných onemocnění nebo poranění pomocí kmenových buněk, neboť jejich…









